Analizaremos las causas conocidas hasta hoy de la esquizofrenia tanto en lo que se refiere a la ETIOLOGÍA como a la FISIOPATOLOGÍA.
¿Por qué se produce la esquizofrenia?
Ya mencionamos la distinción entre:
- ETIOLOGÍA es la ciencia que se centra en el estudio de la causa de la enfermedad, por tanto al origen de la enfermedad, el motivo de porque alguien enferma de esa patología en concreto. Las causas precisas de la esquizofrenia no se conocen, aunque es claro que existen dos conjuntos de factores de riesgo, unos de tipo genético y otros de tipo perinatal, a los que se puede sumar algún factor socioambiental, que podría actuar como precipitante.
- FISIOPATOLOGÍA o PATOGÉNESIS: Hace referencia a los mecanismos anormales característicos en una enfermedad. Los mecanismos fisiopatológicos del trastorno son muy conocidos, y a su vez podemos distinguir entre anormalidades en el sistema de neurotransmisión, anomalías anatómicas y alteraciones del sistema inmune.
ETIOLOGÍA
Factores genéticos
El riesgo de esquizofrenia es elevado en parientes biológicos de personas que la padecen, situándose en el 10% (es decir se multiplica por más de diez el riesgo que sufre la población general). Este riesgo va aumentando en función de la proximidad genética con el paciente, así, si ambos padres sufren esquizofrenia, los hijos tendrán un riesgo del 40% de tener la enfermedad y en gemelos monocigóticos, esta probabilidad alcanza el 50%.
Los estudios de asociación en el genoma humano han identificado varios genes candidatos (en una de las revisiones más recientes la cifra alcanza los 108) pero los hallazgos no siempre se han replicado en diferentes estudios. Como es lógico la mayoría de estos genes se expresan en el cerebro, pero también hay alteraciones en genes relacionados con la inmunidad, dando soporte a la teoría que liga el sistema inmune con esta enfermedad.
A riesgo de parecer una “sopa de letras” mencionaré algunos de estos hallazgos de particular interés:
- El gen COMT que está implicado en la metilación y degradación de los neurotransmisores de tipo catecolamina, como dopamina, adrenalina y noradrenalina.
- El gen RELN que codifica la proteína reelina que a su vez, desempeña un papel en el desarrollo del cerebro y la actividad GABAérgica. En un estudio internacional, una variante común en este gen aumentó el riesgo de esquizofrenia, pero sólo en mujeres.
- El gen NOS1AP codifica la enzima que sintetiza el óxido nítrico, presente en el cerebro como mensajero intracelular en neuronas de tipo inhibidor. Se ha hallado una elevada expresión de este gen en cerebros post-mortem de pacientes que sufrieron esquizofrenia.
- El gen GRM3, codificador de proteínas que también se ha asociado con un riesgo doble o triple de sufrir esquizofrenia, dependencia del alcohol o trastorno bipolar.
- Asimismo, se han descrito múltiples cambios que implican la estructura del gen, como delecciones como las halladas en 1q21.1, 15q13.3 y 22q11.2 y duplicaciones de segmentos de ADN. Estas variantes pueden heredarse, pero también surgir espontáneamente. Todas ellas aumentan el riesgo de desarrollar la enfermedad.
- También se han encontrado anomalías en los genes del neurodesarrollo, como las alteraciones en los genes DISC1, NRG1, DTNBP1, KCNH2, AKT1 y RGS4, dichos cambios se han asociado con la esquizofrenia, aunque con una gran variabilidad entre los diferentes estudios. Asimismo, hay que precisar que algunas personas que sufren la enfermedad no cuentan con antecedentes familiares del trastorno por lo que estos casos pueden ser el resultado de nuevas mutaciones, probablemente en el exoma (la parte de los cromosomas que codifican las proteínas). Diversos estudios han identificado mutaciones genéticas en pacientes con esquizofrenia especialmente en aquellas partes que codifican proteínas específicas implicadas en la función cerebral.Como se desprende de todo lo anterior, es difícil elaborar una hipótesis global que abarque todos los detalles de estos factores genéticos, a los que hay que sumar las interacciones con el medio (tanto interno como externo). No obstante, sofisticados meta-análisis de los estudios realizados con gemelos confirman que estos factores genéticos representarían el 80% de las causas por las que se ha puesto en marcha la enfermedad.Todo ello apoya la hipótesis global de que la esquizofrenia es un trastorno en el que múltiples variantes genéticas conducen a un resultado clínico común.
Factores perinatales
- Aquellos que suceden durante el embarazo y parto:
- Las mujeres que durante su embarazo sufren desnutrición pueden estar en mayor riesgo de dar a luz niños que más tarde desarrollen esquizofrenia. Por ejemplo, los niños nacidos de madres holandesas que estaban desnutridas durante la Segunda Guerra Mundial tuvieron una alta tasa de esquizofrenia.
- El hecho de sufrir infecciones víricas durante el primer y segundo trimestre del embarazo (haciendo hincapié en el virus influenza) también se ha correlacionado con un exceso de casos, más allá de lo esperado estadísticamente. Así sucedió en algunos países tras las epidemias de influenza A2 de 1957.
- Las complicaciones obstétricas (como la asfixia perinatal) pueden estar asociadas con una mayor incidencia de esquizofrenia. o Un hallazgo curioso es que las personas diagnosticadas con esquizofrenia tienen más probabilidades de haber nacido en primavera o invierno, al menos en el hemisferio norte. Y otra relación estadística es que la edad paterna elevada también está asociada con la posibilidad de sufrir la enfermedad.
- Se cree que algunos de estos factores causales pueden provocar una migración neuronal anormal durante el neurodesarrollo, resultando un defecto estructural o bioquímico que se pone en marcha ante precipitantes ambientales en la adolescencia o la edad adulta temprana.
FISIOPATOLOGÍA:
Anomalías del sistema neurotransmisor
Dopamina: 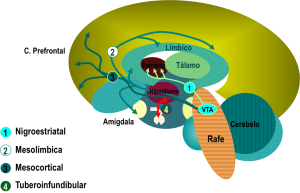
Los pacientes con esquizofrenia sufren anomalías en el sistema de neurotransmisión dopaminérgico. Los fármacos antipsicóticos disminuyen la secreción dopaminérgica en las neuronas mesolímbicas de tipo D2, y por el contrario aquellos productos que estimulan estas neuronas (como por ejemplo las anfetaminas) exacerban los síntomas psicóticos. Sin embargo, las alteraciones en la bioquímica cerebral de la esquizofrenia son más complejas: ya que en determinados momentos coexiste una disminución de la dopamina en el sistema mesocortical (a esto se atribuyen los síntomas negativos) con una actividad hiperdopaminérgica en el sistema mesolímbico (que produciría los delirios y las alucinaciones).
Serotonina:
El neurotransmisor 5-HT y sus subtipos de receptores también se encuentran comprometidos en esta enfermedad (como ocurre con los cuadros depresivos). Se habla de alteraciones de la serotonina durante el desarrollo del sistema nervioso central, de una excesiva activación del cortex prefrontal a través de una alteración del receptor 5-HT2A, o de incluso un desequilibrio entre serotonina y dopamina.
Glutamato:
Se ha descrito una reducción de la funcionalidad de los receptores NMDA de glutamato en pacientes con esquizofrenia, basada en estudios post-mortem y en animales de experimentación. Esta hipótesis se ha visto reforzada por el descubrimiento de varios genes en relación con estás vías glutamatérgicas.
Las diferentes hipótesis sobre dopamina, serotonina y glutamato no son mutuamente excluyentes, ya que los diferentes neurotransmisores regulan la función de otros a través de receptores presinápticos especialmente en vías corticolímbicas. También se han involucrado otros neurotransmisores como la noradrenalina, el GABA, el CCK y diversos neuropéptidos.
Anomalías anatómicas:
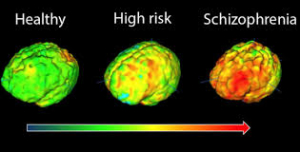
Los estudios de neuroimagen muestran diferencias entre los cerebros de personas que padecen esquizofrenia y sujetos sin el trastorno. Entre los hallazgos verificados, tanto a través de neuroimagen como en estudios postmortem: o Dilatación de los ventrículos laterales, disminución del volumen cerebral en las áreas mediales temporales y cambios en el hipocampo. o Reducción en las redes de conexión de sustancia blanca entre regiones neocorticales y límbicas. o Discreta disminución del volumen total cerebral, especialmente en lóbulos prefrontales y temporales en personas con alto riesgo genético para la esquizofrenia. o Asociación entre los cambios en los lóbulos prefrontales y la gravedad de los síntomas psicóticos. o En un reciente estudio de revisión que comparaba pacientes con esquizofrenia con sujetos control, la enfermedad se asoció con diversas anomalías objetivadas mediante resonancia magnética nuclear, y estas anomalías progresaron con el tiempo.
A considerar que todos estos hallazgos son de mayor interés con fines de investigación que para la aplicación clínica.
Inflamación y función inmune
La función inmunológica se altera en la esquizofrenia. Se especula acerca de que una hiperactivación del sistema inmunológico (como la que se produciría en una infección prenatal) puede conllevar en un exceso de citoquinas inflamatorias y con ello, la consiguiente alteración de la estructura y función cerebral: o Los pacientes con esquizofrenia tienen elevados niveles de citoquinas proinflamatorias que a su vez activan la vía de la cinurenina, mediante la cual el triptófano se metaboliza en ácidos que a su vez regulan la actividad del receptor NMDA y también pueden regular la dopamina.
Los pacientes esquizofrénicos presentan con frecuencia resistencia a la insulina y otros trastornos metabólicos que se han relacionado con la inflamación.